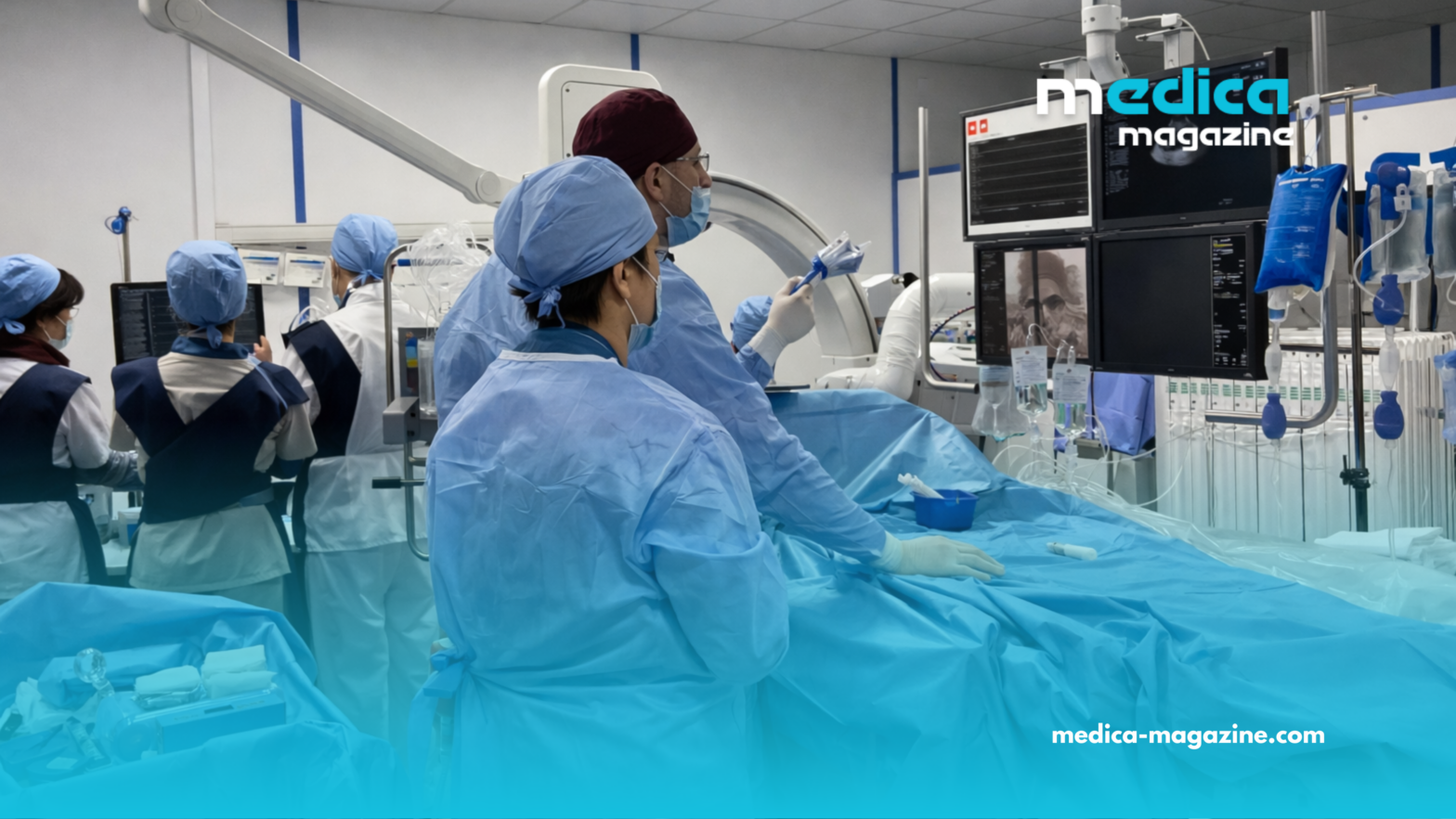
L’intelligence artificielle révolutionne la pratique médicale. Elle améliore les diagnostics, personnalise les traitements et optimise les parcours patients. Cette transformation exige cependant une confiance absolue. La réglementation constitue le pilier central de cette confiance. Elle garantit la sécurité des patients et la viabilité du marché.
Un paysage réglementaire en pleine évolution
Les cadres juridiques doivent s’adapter rapidement aux progrès technologiques. Cette adaptation présente à la fois des défis et des opportunités pour les innovateurs.
Actuellement, le Royaume-Uni régit l’IA médicale sous le régime général des logiciels de dispositifs médicaux. La MHRA travaille à une réforme spécifique via son programme dédié. L’Union européenne, elle, a adopté une loi sur l’IA en 2024. Cette législation s’appliquera pleinement en 2026. Les fabricants britanniques naviguent donc dans une période de transition cruciale.
Les futures exigences intégreront des principes fondamentaux. Parmi eux, figurent le suivi continu des performances et l’explicabilité des modèles. Le Royaume-Uni formalisera d’abord ces concepts via des guides. Une législation spécifique suivra.
LIRE AUSSI : Utilisation de l’intelligence artificielle en santé : Ce que propose l’OMS
Définition et défis spécifiques de l’IA médicale
Un logiciel devient un dispositif médical par sa finalité. S’il contribue aux soins cliniques, la réglementation s’applique. Son objectif est d’assurer l’efficacité, la sécurité et le bon fonctionnement.
L’IA médicale doit respecter les mêmes normes. Cependant, elle introduit des défis uniques :
- Un algorithme peut réagir de façon inattendue à de nouvelles données.
- Ses performances peuvent évoluer avec le temps.
- Des biais peuvent provenir des données d’entraînement.
- La complexité de certains modèles (« boîte noire ») complique la validation.
Normes et conformité : Un guide indispensable
En l’absence de législation britannique définitive, les normes internationales restent la référence. Elles offrent une feuille de route fiable pour les fabricants.
Le respect de plusieurs normes est impératif :
- ISO 13485 pour le management de la qualité.
- IEC 62304 pour le cycle de vie du logiciel médical.
- ISO 14971 pour la gestion des risques.
Cette approche structure le contrôle qualité et l’amélioration continue. Elle permet aussi d’anticiper les futures réglementations et d’éviter des coûts de conformité élevés ultérieurement.
LIRE AUSSI : L’intelligence artificielle révolutionne la caractérisation des stades du cancer du sein
Qualité des données, biais et transparence : Les fondations de la sécurité
La sécurité de l’IA repose d’abord sur la qualité de ses données. Des ensembles de données biaisés ou incomplets génèrent des risques systémiques. Un modèle entraîné sur une population limitée peut sous-performer sur d’autres, créant des inégalités.
Les autorités exigent désormais une traçabilité complète des données. La norme ISO/IEC 5259 sur la qualité des données devient essentielle. Elle définit des caractéristiques clés comme l’exactitude et la crédibilité.
Validation et performance en conditions réelles
Un modèle performant en laboratoire peut l’être moins sur le terrain. Les régulateurs demandent donc des évaluations en conditions cliniques réelles. Ils insistent sur la surveillance post-commercialisation et la protection contre la « dérive » des modèles.
Les fabricants doivent documenter rigoureusement chaque étape. Les registres de risques assurent la traçabilité des décisions. La définition précise du champ d’utilisation prévu est cruciale pour éviter les mauvaises applications.
LIRE AUSSI : L’intelligence artificielle révolutionne la surveillance hospitalière
Collaboration clinique : Une nécessité impérative
L’expertise médicale est indispensable pour interpréter les résultats de l’IA. Un algorithme peut identifier des corrélations trompeuses. Seul un clinicien peut apporter le contexte nécessaire.
Par exemple, un modèle pourrait associer à tort une comorbidité à un meilleur pronostic. En réalité, cette association reflète souvent une prise en charge plus intensive des patients concernés. Sans supervision, l’interprétation serait erronée et dangereuse.
Obstacles pour les innovateurs et perspectives d’avenir
Le principal défi n’est pas toujours technique. Il réside souvent dans l’intégration précoce des exigences réglementaires. Les start-ups, sous pression pour développer un prototype, peuvent reporter cette étape. Cette approche génère ensuite des retards coûteux et bloque les financements.
L’avenir s’oriente vers une réglementation plus robuste et harmonisée au niveau international. La transparence, la surveillance continue et la qualité des données deviendront des piliers incontournables.
En conclusion, la réglementation de l’IA en médecine n’est pas une barrière. C’est le fondement indispensable d’une adoption à grande échelle, sûre et éthique. Elle construit la confiance des patients et des cliniciens, garantissant que l’innovation serve toujours la santé humaine.
LIRE AUSSI : Congrès international de chirurgie endocrinienne et viscérale : Le recours à l’intelligence artificielle mis en avant